Normaalin liekin etenemisnopeus ei riipu. Palamisolosuhteiden vaikutus liekin etenemisnopeuteen
1) Materiaalin kosteus.
2) Näytteen orientaation vaikutus avaruudessa.
Negatiivisilla kaltevuuskulmilla (liekin liikkeen suunta ylhäältä alas) liekin etenemisnopeus joko ei muutu tai pienenee hieman. Kun positiivinen kaltevuuskulma (liekin liikkeen suunta alhaalta ylös) kasvaa yli 10-15 0, liekin etenemisnopeus kasvaa jyrkästi.
3) Ilmavirran nopeuden ja suunnan vaikutus.
Vastatuulen nopeuden kasvaessa kaasunvaihto paranee ja liekin kaltevuus näytteeseen nähden pienenee. Levitysnopeus kasvaa.
Liekin liikesuuntaa vastaan suunnatulla ilmavirralla on kaksinkertainen vaikutus liekin etenemisnopeuteen.
Aerodynaamisen jarrutuksen ja liekin etuosan edessä olevien pinnan kuumennettujen alueiden jäähtymisen seurauksena liekin etenemisnopeus laskee. Toisaalta ilmavirtaus tehostaa pyrolyysituotteiden sekoittumista hapettimeen, homogeenisen palavan seoksen muodostuminen tapahtuu nopeammin, liekin kärki lähestyy kiinteän materiaalin pintaa, mikä puolestaan johtaa edelleen lisääntymiseen. voimakkuus, ja tämä nopeuttaa liekin leviämistä.
4) Näytteen geometristen mittojen vaikutus.
On termisesti paksuja ja termisesti ohuita näytteitä.
Lämpöpaksuus on sen kiinteän materiaalin kerroksen paksuus, joka on kuumennettu liekin etuosan edessä alkulämpötilan yläpuolelle, kun liekki leviää tietylle pinta-alalle.
5) Alustamateriaalin vaikutus.
Jos syttyvä materiaali joutuu kosketuksiin materiaalin (substraatin) kanssa, jonka lämpöfysikaaliset ominaisuudet poikkeavat ilmasta, tämä vaikuttaa myös liekin etenemisnopeuteen (liimapaperi, lankaeristys jne.). Jos l matala > l korkea. matto. , silloin lämpöä poistetaan intensiivisesti näytteestä ja etenemisnopeus on pienempi kuin siinä tapauksessa, että alustaa ei ole.
6) Happipitoisuuden vaikutus ympäristöön.
Kun ympäristön happipitoisuus kasvaa, liekin etenemisnopeus kasvaa.
7. Näytteen alkulämpötilan vaikutus.
Puun osalta alkulämpötilan nousu 230–250 o C:een (pyrolyysin lämpötila-alue) johtaa u l:n voimakkaaseen nousuun.
Kiinteiden materiaalien palaminen
Samanaikaisesti liekin leviämisen kanssa materiaalin pinnalle alkaa palamisprosessi. Kiinteiden materiaalien palamismallit riippuvat merkittävästi kiinteän faasin muuttumisen luonteesta kaasumaisiksi tuotteiksi.
Jos kiinteän faasin hajoaminen tapahtuu kapeassa pinnanläheisessä kerroksessa ilman hiilikerroksen muodostumista, niin tässä tapauksessa palaminen etenee vakionopeudella. Sytytyksen jälkeen kiinteän faasin pinnalle asetetaan vakiolämpötila, joka on yhtä suuri kuin aineen kiehumis- tai sublimaatiolämpötila.
Kiinteiden aineiden palamismekanismi, joka tapahtuu hiilipitoisen jäännöksen muodostuessa palamispinnalle, on monimutkaisempi. Näin palavat lähes kaikki kasviperäiset aineet, osa palamattomia tai hitaasti palavia täyteaineita (talkki, noki jne.) sisältävät muovit. Yleisimmät tämän tyyppiset kasviperäiset palavat aineet ovat puu. Sytytyshetkellä liekkivyöhykkeeltä tulevan lämpövirran vuoksi puun pintakerroksen lämpötila nousee nopeasti 450-500 o C:een. Aineiden intensiivinen hajoaminen tapahtuu haihtuvien tuotteiden ja hiilen muodostuessa, kun taas lämpötila nousee pinnalla lämpötila nousee 600 asteeseen.
Puun polttosyvyyden mukaan on alueita, joilla on erilaiset fysikaaliset ja fysikaalis-kemialliset ominaisuudet. Perinteisesti ne voidaan jakaa 4 vyöhykkeeseen:
I - puuhiili, joka koostuu 99 % hiilestä;
II - puu, jonka pyrolyysiaste vaihtelee;
III - pyrolysoimaton, kuiva puu;
IV - alkuperäinen puu.
Koska puun palamisen aikana kiinteästä faasista vapautuu haihtuvia aineita, materiaali hiiltyy yhä syvemmälle. Hiilipitoisen kerroksen paksuuden lisääntyminen lisää sen lämmönkestävyyttä ja siten hidastaa vielä hajoamattomien puukerrosten kuumenemis- ja pyrolyysinopeutta, ja liekkien palamisnopeus laskee vähitellen. Puun liekkipoltto lakkaa, kun haihtuvien päästöjen massanopeus laskee arvoon 5 g/(m 2 s). Hiilikerroksen paksuus on 15-20 mm.
Puun liekkipolton lakkaaminen avaa ilman hapen pääsyn 650-700 o C lämpötilaan lämmitetylle hiilelle. Puun polton toinen vaihe alkaa - hiilikerroksen heterogeeninen hapettuminen pääosin reaktion mukaan C + O 2 ® CO 2 + 33000 kJ/kg, hiilikerroksen lämpötila nousee 800 o C:een ja heterogeeninen prosessi. hiilen poltto tehostuu entisestään.
Todellinen kuva siirtymisestä homogeenisesta palamisesta heterogeeniseen palamiseen on hieman erilainen kuin esitetty.
Pääasiallinen kiinteiden aineiden palamisprosessia kuvaava kvantitatiivinen parametri on massan palamisnopeus, joka on yksi palon dynamiikan määräävistä parametreista.
Pienennetty massan palamisnopeus on palaneen aineen määrä aikayksikköä kohden tulipalon pinta-alayksikköä kohti.
Metallien poltto
Palamisen luonteen mukaan metallit jaetaan kahteen ryhmään: haihtuviin ja haihtumattomiin.
Haihtuvilla metalleilla on T pl< 1000 К, Т кип < 1500 К. К ним относятся щелочные металлы (литий, натрий, калий и др.) и щелочноземельные (магний, кальций).
Haihtumattomien metallien Tm >1000 K, Tbp >2500 K. Palamismekanismi määräytyy suurelta osin metallioksidin ominaisuuksien mukaan. Haihtuvien metallien sulamispiste on alhaisempi kuin niiden oksidien sulamispiste. Lisäksi jälkimmäiset ovat melko huokoisia muodostelmia.
Kun IR tuodaan metallin pinnalle, se haihtuu ja hapettuu. Kun höyrypitoisuus saavuttaa alemman syttyvän pitoisuusrajan, se syttyy. Diffuusiopolttovyöhyke muodostetaan pintaan, suuri osa lämmöstä siirtyy metalliin ja se kuumennetaan T-kiehumispisteeseen. Tuloksena olevat höyryt, jotka diffundoituvat vapaasti huokoisen oksidikalvon läpi, tulevat palamisalueelle. Metallin kiehuminen aiheuttaa ajoittain oksidikalvon tuhoutumisen, mikä tehostaa palamista. Palamistuotteet (metallioksidit) diffundoituvat paitsi metallin pinnalle edistäen oksidikuoren muodostumista, myös ympäröivään tilaan, jossa ne tiivistyvät ja muodostavat kiinteitä hiukkasia valkoisen savun muodossa. Valkoisen tiheän savun muodostuminen on visuaalinen merkki haihtuvien metallien palamisesta.
Haihtumattomissa metalleissa, joissa on korkea faasimuutoslämpötila, muodostuu poltettaessa pinnalle erittäin tiheä oksidikalvo, joka kiinnittyy hyvin metallin pintaan. Tämän seurauksena metallihöyryn diffuusionopeus kalvon läpi vähenee jyrkästi ja suuret hiukkaset, esimerkiksi alumiini ja beryllium, eivät pysty palamaan. Yleensä tällaisten metallien tulipalot syntyvät, kun ne ovat lastujen, jauheiden ja aerosolien muodossa. Ne palavat tuottamatta tiheää savua. Tiheän oksidikalvon muodostuminen metallipinnalle johtaa hiukkasen räjähtämiseen. Tämä ilmiö, joka havaitaan erityisen usein, kun hiukkaset liikkuvat korkean lämpötilan hapettavassa ympäristössä, liittyy metallihöyryjen kerääntymiseen oksidikalvon alle, jota seuraa sen äkillinen repeämä. Tämä luonnollisesti johtaa palamisen voimakkaaseen tehostumiseen.
Pölyn palaminen
Pöly on dispergoitu järjestelmä, joka koostuu kaasumaisesta dispersioväliaineesta (ilma jne.) ja kiinteästä dispergoidusta faasista (jauhot, sokeri, puu, kivihiili jne.).
Liekin etenemisnopeuteen vaikuttavat tekijät pöly-ilmaseosten läpi:
1) Pölypitoisuus.
Kuten homogeenisen kaasu-ilma-seoksen palamisen tapauksessa, suurin liekin etenemisnopeus esiintyy seoksilla, jotka ovat hieman korkeammat kuin stoikiometrinen koostumus. Turvepölylle se on 1,0-1,5 kg/m3.
2) Tuhkapitoisuus.
Tuhkapitoisuuden kasvaessa palavan komponentin pitoisuus pienenee ja vastaavasti liekin etenemisnopeus pienenee.
Kun happipitoisuus pienenee, liekin etenemisnopeus hidastuu.
Pölyjen luokitus palo- ja räjähdysvaaran mukaan.
Palo- ja räjähdysvaaran perusteella pölyt jaetaan luokkiin:
Luokka I - räjähtävin - j n enintään 15 g/m 3;
Luokka II - räjähtävä - 15 g/m 3< j н < 65 г/м 3 ;
Luokka III - palovaarallisin - j n > 65 g/m 3 ; T St 250 o C asti;
IV luokka - palovaarallinen - j n > 65 g/m 3 ; T St > 250 o C.
PALON KEHITTYMISEN DYNAMIIKKA
Tulidynamiikka ymmärretään joukkona lakeja ja malleja, jotka kuvaavat muutoksia tulipalon pääparametreissa ajassa ja tilassa. Tulipalon luonne voidaan arvioida useiden sen parametrien yhdistelmällä: palon pinta-ala, palon lämpötila, sen leviämisnopeus, lämmön vapautumisen intensiteetti, kaasunvaihdon intensiteetti. , savun voimakkuus jne.
Paloparametreja on niin monia, että joissakin palotyypeissä osa niistä on ensisijaisia ja toisissa toissijaisia. Kaikki riippuu siitä, mitä tavoitteita tietyn tulipalon tutkimiselle on asetettu.
Tulipalon dynamiikan tutkimiseksi otamme palon pinta-alan, tulen lämpötilan, kaasunvaihdon ja savun voimakkuuden sekä palon leviämisnopeuden tärkeimmiksi ajan myötä muuttuviksi parametreiksi. Nämä paloparametrit ovat parhaiten käytettävissä mittauksia, analyysejä ja laskelmia varten. Ne toimivat lähtötietoina tarvittavien laitteiden tyypin määrittämisessä ja voimien ja keinojen laskemisessa tulipalojen sammutuksessa, automaattisten sammutusjärjestelmien suunnittelussa jne.
Tulipalon syttymishetkestä sen vapaalla kehittymisellä sen täydelliseen sammumiseen asti, huoneessa oleva tulipalo voidaan jakaa vaiheisiin.
Palon vaiheet
I. Sytytysvaihe.
Liekki syntyy ulkoisesta sytytyslähteestä pienellä alueella ja leviää hitaasti. Polttovyöhykkeen ympärille muodostuu konvektiivinen kaasuvirtaus, joka varmistaa tarvittavan kaasunvaihdon. Palavan materiaalin pinta lämpenee, polttimen koko kasvaa, kaasunvaihto lisääntyy ja säteilylämpövirta kasvaa, joka tulee ympäröivään tilaan ja palavan materiaalin pinnalle. Rusketusvaiheen kesto on 1-3 minuuttia.
II. Palon käynnistysvaihe.
Huoneen lämpötila nousee hitaasti. Koko edellinen prosessi toistetaan, mutta suuremmalla intensiteetillä. Toisen vaiheen kesto on noin 5-10 minuuttia.
III. Volumetrisen tulipalon kehitysvaihe- kaikkien lueteltujen parametrien nopea kasvuprosessi. Huoneen lämpötila saavuttaa 250 - 300 °C. Palon kehittymisen "volumetrinen" vaihe ja tulipalon volumetrisen leviämisen vaihe alkaa. Kun kaasun lämpötila huoneessa on 300°C, lasitus tuhoutuu. Jälkipoltto voi tapahtua myös huoneen ulkopuolella (palo karkaa aukoista ulos). Kaasunvaihdon intensiteetti muuttuu äkillisesti: se kasvaa jyrkästi, kuumien palamistuotteiden ulosvirtausprosessi ja raikkaan ilman virtaus palamisalueelle voimistuu.
IV. Palovaihe.
Tämän vaiheen aikana huonelämpötila saattaa laskea hetkellisesti. Mutta kaasunvaihto-olosuhteiden muutoksen mukaisesti paloparametrit, kuten palamisen täydellisyys, palamisnopeus ja palamisprosessin leviäminen, kasvavat jyrkästi. Näin ollen kokonaislämmön vapautuminen tulipalon aikana kasvaa jyrkästi. Lämpötila, joka laski hieman lasin tuhoutumishetkellä kylmän ilman sisäänvirtauksen vuoksi, nousee jyrkästi saavuttaen 500 - 600 ° C. Palon kehittymisprosessi kiihtyy nopeasti. Kaikkien aiemmin mainittujen paloparametrien numeerinen arvo kasvaa. Tulipalon pinta-ala, huoneen keskimääräinen tilavuuslämpötila (800-900 °C), palokuorman palamisen voimakkuus ja savuaste saavuttavat maksiminsa.
V. Kiinteä palamisvaihe.
Paloparametrit ovat vakiintumassa. Tämä tapahtuu yleensä 20-25 minuutin kuluttua tulipalosta ja voi kestää palokuorman koosta riippuen 20-30 minuuttia.
VI. Hajoamisvaihe.
Palamisintensiteetti laskee vähitellen, koska suurin osa palokuormasta on jo palanut. Huoneeseen oli kertynyt suuri määrä palamistuotteita. Huoneen hapen keskimääräinen tilavuuspitoisuus laski 16-17 %:iin ja intensiivistä palamista estävien palamistuotteiden pitoisuus nousi maksimiarvoon. Säteilylämmönsiirron intensiteetti palavaan materiaaliin laski palamisvyöhykkeen lämpötilan laskun vuoksi. Väliaineen optisen tiheyden lisääntymisen vuoksi palamisintensiteetti laskee hitaasti, mikä johtaa kaikkien muiden paloparametrien laskuun. Paloalue ei kutistu: se voi kasvaa tai vakiintua.
VII. Jälkipolttovaihe.
Tälle tulen loppuvaiheelle on ominaista hidas kyteminen, jonka jälkeen palaminen lakkaa jonkin, joskus melko pitkän ajan kuluttua.
Palon perusparametrit
Tarkastellaanpa kvantitatiivisesti joitain tulipalon pääparametreja, jotka määräävät sen kehityksen dynamiikan. Määritetään lämmön vapautumisen intensiteetti tulipalossa, koska tämä on yksi palamisprosessin pääparametreista:
Q=βQ р n V m ’Sp, (kJ/s)
missä β ja Q р n ovat vakioita (alipolttokerroin ja palokuorman alempi lämpöarvo);
V m¢ - alennettu massan palamisnopeus;
S p – paloalue;
V m ¢ ja S p riippuvat palon kehittymisajasta, palolämpötilasta, kaasun vaihtonopeudesta jne.
Alennettu massan palamisnopeus V m ¢ määritetään kaavalla:
v m¢ = (a × T p + b × I g) v m o ¢
jossa a, b ovat empiirisiä kertoimia;
v m o ¢ - palokuorman palamisen pienentynyt massanopeus tietyntyyppiselle palavan materiaalin osalta;
T p - keskimääräinen palolämpötila;
I g - kaasunvaihdon intensiteetti.
Paloalueen riippuvuus sen kehityksen pääparametreista on muotoa:
S p = k (v p ∙ τ) n
jossa k ja n ovat paloalueen geometrisesta muodosta riippuvia kertoimia;
v р – palon lineaarinen leviämisnopeus;
τ on sen vapaan kehityksen aika.
k = π; n = 2 k = ; n = 2 k = 2a; n = 1
k = ; n = 2 k = 2a; n = 1
Palon lineaarinen etenemisnopeus riippuu palavan kuorman tyypistä, palon keskilämpötilasta ja kaasunvaihdon voimakkuudesta:
v p = (a 1 T p + b 1 I g) v po
jossa a 1 ja b 1 ovat empiirisiä kertoimia, jotka määrittävät palon lineaarisen leviämisnopeuden riippuvuuden keskilämpötilasta ja kaasunvaihdon intensiteetistä ja joiden numeerinen arvo määritetään empiirisesti kullekin tietylle polttoainetyypille;
v p o - palamisen lineaarinen etenemisnopeus tietylle polttoainetyypille.
Palon kehittyessä palon lämpötila ja kaasunvaihtonopeus kasvavat, mikä lisää palamisen lineaarista etenemisnopeutta ja pienentää massan palamisnopeutta.
Lämpöolosuhteet tulipalon aikana
Lämpöprosessien esiintyminen ja nopeus riippuvat lämmön vapautumisen voimakkuudesta paloalueella, ts. tulen kuumuudesta. Tulipalossa tapahtuvan lämmön vapautumisen muutosten kvantitatiivinen ominaisuus erilaisista palamisolosuhteista riippuen on lämpötilajärjestelmä. Tulipalon lämpötilajärjestelmällä tarkoitetaan lämpötilan muutosta ajan kuluessa. Palolämpötilan määrittäminen sekä kokeellisesti että laskennallisesti on erittäin vaikeaa. Teknisiä laskelmia varten, kun ratkaistaan useita käytännön ongelmia, palolämpötila määritetään lämpötasapainoyhtälöstä. Tulipalon lämpötasapainoa ei laadita ainoastaan palon lämpötilan määrittämiseksi, vaan myös lämpöenergian määrällisen jakautumisen tunnistamiseksi. Yleensä tulipalon lämpötasapaino tietyllä hetkellä voidaan esittää seuraavasti:
Q p = Q pg + Q k + Q l
missä Q p on tulipalossa vapautuva lämpö, kJ;
Q pg - palamistuotteiden sisältämä lämpö, kJ;
Q к - lämpö, joka siirtyy palamisvyöhykkeeltä konvektiolla vyöhykettä pesevään ilmaan, mutta ei osallistu palamiseen, kJ;
Q l – säteilyn kautta palamisvyöhykkeeltä siirtynyt lämpö.
Avopalojen osalta on todettu, että palamisvyöhykkeeltä säteilyn ja konvektion kautta siirtyvän lämmön osuus on 40-50 % Q p:stä Loput lämmöstä (60-70 % Q p:stä) käytetään palamisen lämmittämiseen Tuotteet. Siten 60-70 % tietyn palavan materiaalin teoreettisesta palamislämpötilasta antaa likimääräisen liekin lämpötilan arvon. Avotulen lämpötila riippuu palavien materiaalien lämpöarvosta, palamisnopeudesta ja sääolosuhteista. Keskimäärin avotulen maksimilämpötila palaville kaasuille on 1200 - 1350°C, nesteille - 1100 - 1300°C ja orgaanista alkuperää oleville kiinteille palaville materiaaleille - 1100 - 1250°C.
Sisäpalossa lämpötilaan vaikuttavat useampi tekijä: palavan materiaalin luonne, palokuorman suuruus ja sijainti, palamisalue, rakennuksen mitat (lattiapinta-ala, huoneen korkeus jne.) ja kaasunvaihdon intensiteetti (aukkojen koko ja sijainti). Tarkastellaanpa tarkemmin näiden tekijöiden vaikutusta.
Tulipalo voidaan jakaa kolmeen ominaiseen ajanjaksoon lämpötilan muutosten perusteella: alku-, pää- ja loppujakso.
Alkujakso- jolle on ominaista suhteellisen alhainen keskimääräinen tilavuuden lämpötila.
Pääkausi- sen aikana palaa 70-80% palavien materiaalien kokonaiskuormasta. Tämä ajanjakso päättyy, kun tilavuuden keskilämpötila saavuttaa maksimiarvonsa tai laskee enintään 80 prosenttiin maksimiarvostaan.
Viimeinen ajanjakso- ominaista lämpötilan lasku palokuorman palamisen vuoksi.

Kuva 9.1. Sisäisen tulipalon lämpötilan muutos ajan kuluessa: 1 - tietyn tulipalon käyrä; 2 - vakiokäyrä
Koska palolämpötilan kasvunopeudella ja itseisarvolla kussakin tapauksessa on omat ominaisarvonsa ja ominaisuutensa, otettiin käyttöön vakiolämpötilakäyrän käsite (kuva 21.2), joka tiivistää palolämpötilan muutosten tyypillisimpiä piirteitä. sisäisten tulipalojen lämpötila. Standardilämpötila kuvataan yhtälöllä.
Laminaarin palamisnopeus – nopeus, jolla liekin etuosa liikkuu suunnassa, joka on kohtisuorassa tuoreen polttoainenipun pintaan nähden.
 – laminaarinen paloalue;
– laminaarinen paloalue;
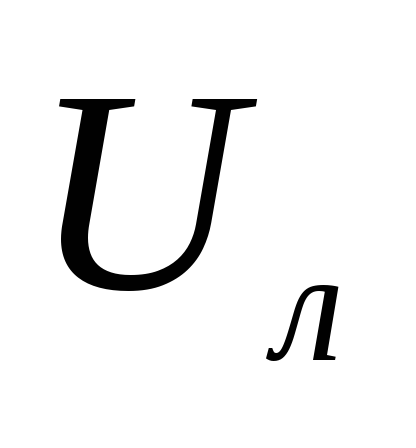 – laminaarisen palamisen nopeus.
– laminaarisen palamisen nopeus.
Turbulentti palaminen.

Turbulentti liekin nopeus – nopeus, jolla liekinrintama liikkuu turbulenttisessa virtauksessa.
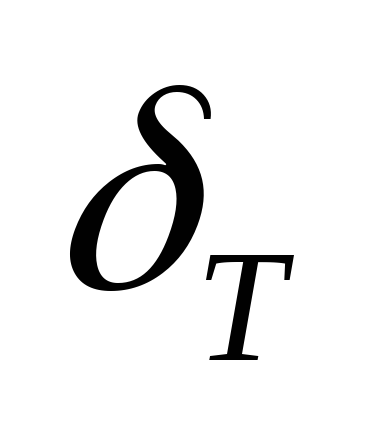 – turbulenttinen paloalue;
– turbulenttinen paloalue;

 – pienten hiukkasten normaalit nopeudet.
– pienten hiukkasten normaalit nopeudet.
Laminaaripoltto ei tuota vaadittua lämmön vapautumisnopeutta moottorissa, joten kaasuvirtauksen turbulenssia tarvitaan.
Arrheniuksen yhtälö:
 – kemiallisen reaktion nopeus.
– kemiallisen reaktion nopeus.
 – kemiallinen reaktiovakio seoksen koostumuksesta ja polttoainetyypistä riippuen;
– kemiallinen reaktiovakio seoksen koostumuksesta ja polttoainetyypistä riippuen;
 – kemiallisen reaktion paine;
– kemiallisen reaktion paine;
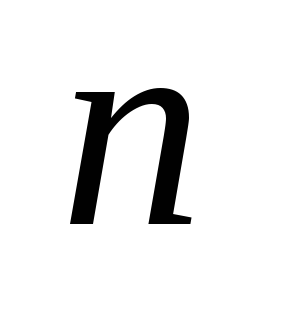 – kemiallisen reaktion järjestys;
– kemiallisen reaktion järjestys; 
 -yleiskaasuvakio;
-yleiskaasuvakio;
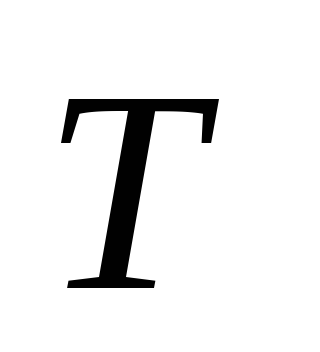 – kemiallisen reaktion lämpötila;
– kemiallisen reaktion lämpötila;
 – Aktivointienergia on energiaa, joka tarvitaan molekyylin sisäisten sidosten katkaisemiseen.
– Aktivointienergia on energiaa, joka tarvitaan molekyylin sisäisten sidosten katkaisemiseen.
Eri tekijöiden vaikutus polttoprosessiin kipinäsytytteisessä polttomoottorissa.
Seoksen koostumus.
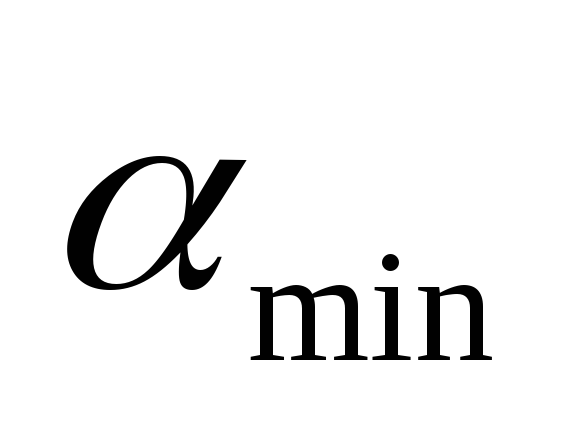
 – yläpitoisuusraja;
– yläpitoisuusraja;
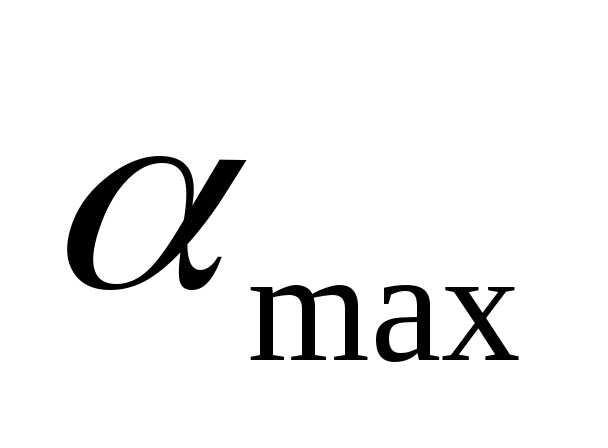 – alempi pitoisuusraja;
– alempi pitoisuusraja;
 – normaali palaminen;
– normaali palaminen;
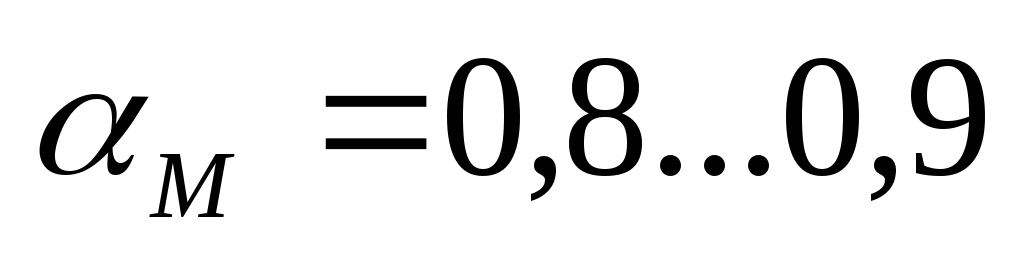
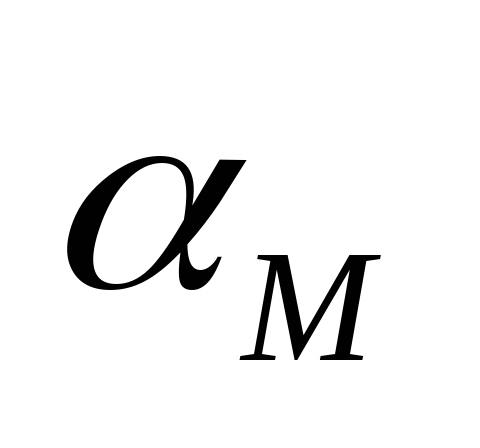 –seoksen tehokoostumus
– moottorin kehittämä suurin teho.
–seoksen tehokoostumus
– moottorin kehittämä suurin teho.

 –seoksen taloudellinen koostumus
– maksimaalinen tehokkuus.
–seoksen taloudellinen koostumus
– maksimaalinen tehokkuus.
Puristussuhde.



Nopeuden kasvaessa sytytysvaihe kasvaa, mikä johtaa palamisprosessin myöhäiseen kehittymiseen ja sykliä kohti vapautuvan lämmön määrän vähenemiseen. Siksi vaihtaessa  sytytysajoituksen (IPA) säätö vaaditaan.
sytytysajoituksen (IPA) säätö vaaditaan.
Sytytyksen ajoitus.
Sytytyksen ajoitus – kampiakselin kiertokulma siitä hetkestä lähtien, kun kipinä syötetään TDC:hen.
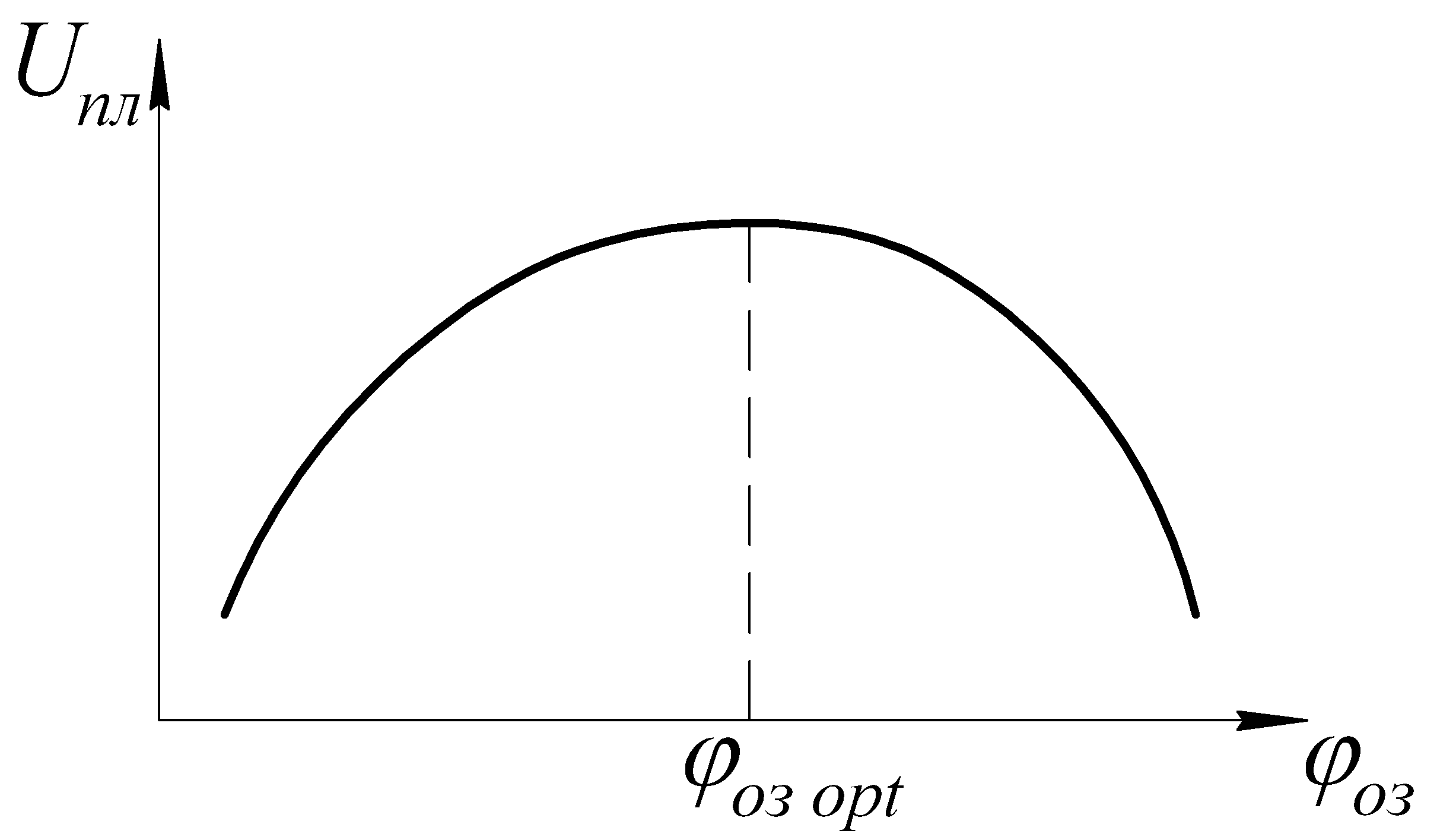
P  kuormituksen alla
ymmärrä kaasuventtiilin kiertokulma - tämä säätelee moottorin kuormitusta.
kuormituksen alla
ymmärrä kaasuventtiilin kiertokulma - tämä säätelee moottorin kuormitusta.
 – kaasuventtiilin kiertokulma.
– kaasuventtiilin kiertokulma.
Tärkeimmät häiriöt kipinäsytytteisten polttomoottoreiden palamisprosessissa. Räjähdys.
D  etonaatio
– seoksen räjähdysmäinen palaminen, johon liittyy paineaallot, jotka leviävät koko polttokammion tilavuudessa. Räjähdys tapahtuu sytytystulpan ulkopuolella olevien seoksen osien itsesyttymisen seurauksena, mikä johtuu voimakkaasta kuumenemisesta ja puristamisesta liekin etuosan etenemisen aikana.
etonaatio
– seoksen räjähdysmäinen palaminen, johon liittyy paineaallot, jotka leviävät koko polttokammion tilavuudessa. Räjähdys tapahtuu sytytystulpan ulkopuolella olevien seoksen osien itsesyttymisen seurauksena, mikä johtuu voimakkaasta kuumenemisesta ja puristamisesta liekin etuosan etenemisen aikana.

Räjäytyksen yhteydessä: 
Polttokammion seinistä heijastuva iskuaalto muodostaa toissijaisia liekkirintamia ja itsesyttymislähteitä. Ulkoisesti räjähdys ilmenee tylsinä nakutuksena, kun moottori käy raskaalla kuormituksella.
Moottorin toiminnan seuraukset räjähdyksen kanssa:
Yksittäisten moottorin osien (venttiilit, männät, pään tiivisteet, sytytystulpan elektrodit) ylikuumeneminen ja palaminen;
Moottorin osien mekaaninen tuhoutuminen iskukuormituksen vuoksi;
Vähentynyt teho ja tehokkuus.
Että. Pitkäaikainen työskentely räjäytyksellä ei ole hyväksyttävää.
P  Tässä ovat tekijät, jotka aiheuttavat räjähdyksen:
Tässä ovat tekijät, jotka aiheuttavat räjähdyksen:

Polttoaineen kyky syttyä itsestään on ominaista räjähdyskestävyys , ja räjähdysvastus on arvioitu oktaaniluku (OC) .
ERITTÄIN – on numeerisesti yhtä suuri kuin huonosti ditonoivan isooktaanin tilavuusosuus seoksessa helposti ditonoivan normaalin heptaanin kanssa, mikä vastaa räjähdysominaisuuksiltaan tätä bensiiniä.
Isooktaani – 100 yksikköä, normaali heptaani – 0 yksikköä.
Esimerkiksi: Oktaaniluku 92 tarkoittaa, että tällä bensiinillä on sama iskunkesto kuin vertailuseoksella, jossa on 92 % isooktaania ja 8 % normaalia heptaania.
A  - moottoribensiini;
- moottoribensiini;
ja – tutkimusmenetelmä bensiinin saamiseksi;
m – moottorimenetelmä (kirjainta ei yleensä kirjoiteta).
Moottoritutkimusmenetelmässä puristussuhdetta säädetään, kunnes räjähdys alkaa, ja oktaaniluku määritetään taulukoista.
Motoriset menetelmät simuloida ajoa täydellä kuormalla (rekka kaupungin ulkopuolella).
Tutkimusmenetelmä simuloi ajamista osakuormalla (kaupungissa).


Jos oktaaniluku on liian korkea, liekin etenemisnopeus laskee. Palamisprosessi viivästyy, mikä johtaa tehokkuuden laskuun ja pakokaasun lämpötilan nousuun. Seurauksena on tehon lasku, lisääntynyt polttoaineenkulutus, moottorin ylikuumeneminen ja yksittäisten elementtien palaminen. Moottorin suurin suorituskyky saavutetaan, kun polttoaineen oktaaniluku on lähellä räjähdyskynnystä.
Tapoja torjua räjähdyksiä:

Nestemäisen tai kiinteän aineen pinnan yläpuolella missä tahansa lämpötilassa on höyry-ilmaseos, jonka paine tasapainotilassa määräytyy tyydyttyneiden höyryjen paineen tai niiden pitoisuuden perusteella. Lämpötilan noustessa kylläisen höyryn paine kasvaa eksponentiaalisesti (Clapeyron-Clausis-yhtälö):
missä Р n „ - kylläisen höyryn paine, Pa; Q„ C11 - haihdutuslämpö, kJ/mol; T - nesteen lämpötila, K.
Kaikille nesteille on olemassa lämpötila-alue, jossa tyydyttyneiden höyryjen pitoisuus peilin (nesteen pinnan) yläpuolella on sytytysalueella, ts. NKPV
Höyryn LTPV:n luomiseksi riittää, ettei koko nestettä lämmitetä, vaan vain sen pintakerros lämpötilaan, joka on yhtä suuri kuin LTPV.
Sytytyslähteen läsnä ollessa tällainen seos voi syttyä. Käytännössä käsitteitä "leimahduspiste" ja "syttymislämpötila" käytetään useammin.
Leimahduspiste on nesteen vähimmäislämpötila, jossa sen pinnan yläpuolelle muodostuu sellainen höyrypitoisuus, joka pystyy syttymään sytytyslähteestä, mutta höyryn muodostumisnopeus ei riitä ylläpitämään palamista.
Siten sekä leimahduspisteessä että syttymislämpötilan alarajassa nesteen pinnan yläpuolelle muodostuu syttymisen alempi pitoisuusraja, mutta jälkimmäisessä tapauksessa LFL syntyy kylläisen höyryn vaikutuksesta. Siksi leimahduspiste on aina hieman korkeampi kuin LTPV. Vaikka leimahduspisteessä tapahtuu lyhytkestoista höyryjen syttymistä, joka ei pysty kehittymään nesteen stabiiliksi palamiseksi, leimahdus voi kuitenkin tietyissä olosuhteissa aiheuttaa tulipalon.
Leimahduspiste otetaan perustana nesteiden luokittelulle palaviin nesteisiin (FLL) ja syttyviin nesteisiin (CL). Nesteet, joiden leimahduspiste suljetussa astiassa on 61 °C tai alhaisempi, luokitellaan palaviksi nesteiksi, kun taas palaviin nesteisiin kuuluvat ne, joiden leimahduspiste on yli 61 °C.
Leimahduspiste määritetään kokeellisesti avoimen ja suljetun tyyppisissä laitteissa. Suljetuissa astioissa leimahduspistearvot ovat aina alhaisemmat kuin avoimissa, koska tällöin nestehöyryt voivat diffundoitua ilmakehään ja korkeampaa lämpötilaa tarvitaan syttyvän pitoisuuden muodostamiseksi pinnan yläpuolelle.
Taulukossa 2.4 näyttää joidenkin nesteiden leimahduspisteen avoimilla ja suljetuilla instrumenteilla.
Taulukko 2.4
Erityyppisten nesteiden leimahduspiste erilaisilla määritysmenetelmillä
Syttymislämpötila on nesteen vähimmäislämpötila, jossa sytytyslähteestä peräisin olevien höyryjen syttymisen jälkeen saadaan aikaan tasainen palaminen.
Syttyvien nesteiden syttymislämpötila on 1-5° korkeampi kuin leimahduspiste, kun taas mitä matalampi leimahduspiste, sitä pienempi ero syttymis- ja leimahduspisteiden välillä on.
Syttyvillä nesteillä, joilla on korkea leimahduspiste, näiden lämpötilojen ero on 25-35°. Suljetun upokkaan leimahduspisteen ja syttymislämpötilan alemman rajan välillä on korrelaatio, joka kuvataan kaavalla
Tämä suhde pätee ГВ(.
Leimahdus- ja syttymislämpötilojen merkittävä riippuvuus koeolosuhteista aiheuttaa tiettyjä vaikeuksia laskentamenetelmän luomisessa niiden arvojen arvioimiseksi. Yksi yleisimmistä niistä on V. I. Blinovin ehdottama puoliempiirinen menetelmä:
missä G aurinko on salaman (sytytys) lämpötila, K; R np - nesteen kylläisen höyryn osapaine leimahdus- (sytytys)lämpötilassa, Pa; D()- nestehöyryn diffuusiokerroin, s/m 2 ; b- happimolekyylien lukumäärä, joka tarvitaan yhden polttoainemolekyylin täydelliseen hapettumiseen; SISÄÄN - määritysmenetelmän vakio.
Laskettaessa leimahduspistettä suljetussa astiassa on suositeltavaa ottaa SISÄÄN= 28, avoimessa astiassa SISÄÄN= 45; sytytyslämpötilan laskemiseksi ota SISÄÄN = 53.
Syttyvien lämpötilojen rajat voidaan laskea:
Perustuu tunnettuihin kiehumispistearvoihin
missä ^н(в)’ 7/ip - syttymislämpötilan alempi (ylempi) raja ja kiehumispiste, °C; k, minä - parametrit, joiden arvot riippuvat syttyvän nesteen tyypistä;
Perustuu tunnettuihin pitoisuusrajojen arvoihin. Tätä varten määritä ensin tyydyttyneiden höyryjen pitoisuus nesteen pinnan yläpuolella
missä (p„ p on tyydyttyneiden höyryjen pitoisuus, %; R n n - kylläisen höyryn paine, Pa; P 0 - ulkoinen (ilmakehän) paine, Pa.
Kaavasta (2.41) seuraa
Määritettyämme kylläisen höyryn paineen alemman (ylemmän) syttymisrajan arvosta, löydämme lämpötilan, jossa tämä paine saavutetaan. Se on syttymislämpötilan alempi (ylempi) raja.
Kaavan (2.41) avulla voit myös ratkaista käänteisen ongelman: laske syttymisen pitoisuusrajat tunnettujen lämpötilarajojen arvojen perusteella.
Liekin ominaisuus spontaanisti leviämisen havaitaan paitsi palavien kaasujen seosten palamisen aikana hapettimen kanssa, myös nesteitä poltettaessa Ja kiinteät aineet. Altistuessaan paikallisesti lämmönlähteelle, esimerkiksi avotulelle, neste lämpenee, haihtumisnopeus kasvaa ja kun nesteen pinta saavuttaa syttymislämpötilan lämmönlähteen vaikutuskohdassa, höyry- ilmaseos syttyy, muodostuu vakaa liekki, joka sitten leviää tietyllä nopeudella pitkin pintaa ja kylmän osan nesteitä.
Mikä on palamisprosessin leviämisen liikkeellepaneva voima, mikä on sen mekanismi?
Liekin eteneminen nesteen pinnalla tapahtuu säteilyn, konvektion ja molekyylilämmönjohtavuuden aiheuttaman lämmönsiirron seurauksena liekkivyöhykkeeltä nestepeilin pinnalle.
Nykyaikaisten käsitteiden mukaan palamisprosessin etenemisen pääasiallinen voima on liekin lämpösäteily. Liekin, jolla on korkea lämpötila (yli 1000 °C), tiedetään pystyvän säteilemään lämpöenergiaa. Stefan-Boltzmannin lain mukaan kuumennetun kappaleen lähettämän säteilylämpövuon intensiteetti määräytyy suhteessa
Missä ts i- säteilylämpövirran intensiteetti, kW/m 2 ; 8 0 - rungon mustuusaste (liekki) (e 0 = 0,75-H,0); a = = 5,7 10 11 kJ/(m 2 s K 4) - Stefan-Boltzmannin vakio; G g - kehon (liekin) lämpötila, K; G 0 - keskilämpötila, K.
Lämpö, joka säteilee kaikkiin suuntiin, saavuttaa osittain nesteen pinnan alueet, jotka eivät ole vielä syttyneet, lämmittäen niitä. Lämmitettävän alueen yläpuolella olevan pintakerroksen lämpötilan noustessa nesteen haihtumisprosessi voimistuu ja muodostuu höyry-ilma-seos. Heti kun nestehöyryn pitoisuus ylittää LVEL-arvon, se syttyy liekistä. Sitten tämä nestepinnan osa alkaa intensiivisesti lämmittää nestepinnan viereistä osaa jne. Liekin etenemisnopeus nesteen läpi riippuu nesteen pinnan kuumenemisnopeudesta liekistä tulevan säteilylämpövuon vaikutuksesta, ts. syttyvän höyry-ilmaseoksen muodostumisnopeudesta nesteen pinnan yläpuolelle, mikä puolestaan riippuu nesteen laadusta ja alkulämpötilasta.
Jokaisella nestetyypillä on oma haihtumislämpö ja leimahduspiste. Mitä korkeammat arvot ovat, sitä pidempi aika kuluu sen lämpenemiseen ennen palavan höyry-ilmaseoksen muodostumista, sitä pienempi liekin etenemisnopeus. Kun aineen molekyylipaino kasvaa yhden homologisen sarjan sisällä, elastinen höyrynpaine laskee, haihtumislämpö ja leimahduspiste kasvavat ja liekin etenemisnopeus pienenee vastaavasti.
Nesteen lämpötilan nostaminen lisää liekin etenemisnopeutta, koska aika, joka tarvitaan nesteen lämpenemiseen leimahduspisteeseensä ennen kuin palamisvyöhyke pienenee.
Välähdyksen aikana liekin etenemisnopeus nesteen pintaa pitkin on (fysikaalisessa mielessä) yhtä suuri kuin liekin etenemisnopeus LCPV:tä lähellä olevan koostumuksen höyry-ilmaseoksen läpi, ts. 4-5 cm/s. Kun nesteen alkulämpötila nousee leimahduspisteen yläpuolelle, liekin etenemisnopeus riippuu (samalla tavalla kuin liekin etenemisnopeus) palavan seoksen koostumuksesta. Itse asiassa, nesteen lämpötilan noustessa sen leimahduspisteen yläpuolelle, höyry-ilmaseoksen pitoisuus peilin pinnan yläpuolella nousee LVVP:stä 100 prosenttiin (kiehumispiste).
Näin ollen, aluksi, kun nesteen lämpötila nousee leimahduspisteestä lämpötilaan, jossa pinnan yläpuolelle muodostuu tyydyttyneitä höyryjä pitoisuudella, joka on yhtä suuri kuin stökiömetrinen (tarkemmin hieman suurempi kuin stoikiometrinen), liekin nopeus. lisääntyminen lisääntyy. Suljetuissa astioissa nesteen lämpötilan noustessa edelleen liekin etenemisnopeus alkaa laskea syttymislämpötilan ylärajaa vastaavaan nopeuteen, jossa liekin ja höyry-ilmaseoksen leviäminen ei enää tapahdu. olla mahdollista nesteen pinnan yläpuolella olevan höyry-ilmaseoksen hapen puutteen vuoksi. Avoimen säiliön pinnan yläpuolella höyryn pitoisuus eri tasoilla on erilainen: pinnalla se on maksimi ja vastaa tyydyttyneen höyryn pitoisuutta tietyssä lämpötilassa, kun etäisyys pinnasta kasvaa, pitoisuus kasvaa vähitellen konvektiivisesta ja molekyylidiffuusiosta johtuen.
Nestelämpötilassa, joka on lähellä leimahduspistettä, liekin etenemisnopeus nesteen pintaa pitkin on yhtä suuri kuin sen etenemisnopeus ilmassa olevan höyryseoksen läpi LCPV:ssä, ts. 3-4 cm/s. Tässä tapauksessa liekin etuosa sijaitsee nesteen pinnalla. Nesteen alkulämpötilan noustessa edelleen liekin etenemisnopeus kasvaa samalla tavalla kuin normaalin liekin etenemisnopeuden kasvu höyry-ilmaseoksen läpi sen pitoisuuden kasvaessa. Suurimmalla nopeudella liekki leviää seoksen läpi pitoisuudella, joka on lähellä stoikiometristä. Näin ollen nesteen alkulämpötilan noustessa Gstx:n yläpuolelle liekin etenemisnopeus pysyy vakiona, yhtä suurena kuin palamisen etenemisnopeuden maksimiarvo stoikiometrisen seoksen läpi tai hieman sitä suurempana (kuva 2.5). Täten,

Riisi. 25.
1 - nesteen polttaminen suljetussa astiassa; 2 - nesteen palaminen avoimessa astiassa, kun nesteen alkulämpötila avoimessa säiliössä muuttuu laajalla lämpötila-alueella (kiehumispisteeseen asti), liekin etenemisnopeus vaihtelee useista millimetreistä 3-4 m/ s.
Suurimmalla nopeudella liekki leviää seoksen läpi pitoisuudella, joka on lähellä stoikiometristä. Nesteen lämpötilan noustessa Gstx:n yläpuolelle etäisyys nesteen yläpuolelle, jossa muodostuu stoikiometrinen pitoisuus, kasvaa ja liekin etenemisnopeus pysyy samana (ks. kuva 2.5). Tämä seikka on aina muistettava, niin ennaltaehkäisevää työtä järjestettäessä kuin tulipaloa sammutettaessa, kun esimerkiksi voi olla vaara, että ilma pääsee vuotamaan suljettuun astiaan - sen paineenalennus.
Kun neste syttyy ja liekki leviää, sen pinta muuttuu sen palamisen diffuusiotila, jolle on ominaista ominaismassa W rM ja lineaarinen W V Jl nopeudet.
Ominaismassanopeus on nestepeilin pinta-alayksiköltä palaneen aineen massa aikayksikköä kohti (kg/(m 2 *s)).
Lineaarinen nopeus on etäisyys, jolla nestepinnan taso liikkuu aikayksikössä sen palamisen vuoksi (m/s).
Massa- ja lineaariset palamisnopeudet liittyvät toisiinsa nestetiheyden p kautta:
Nesteen syttyessä sen pintalämpötila nousee syttymislämpötilasta kiehumispisteeseen ja muodostuu kuumennettu kerros. Tänä aikana nesteen palamisnopeus kasvaa vähitellen, liekin korkeus kasvaa riippuen säiliön halkaisijasta ja palavan nesteen tyypistä. 1-10 minuutin palamisen jälkeen prosessi stabiloituu: palamisnopeus ja liekin koko pysyvät muuttumattomina jatkossa.
Liekin korkeus ja muoto nesteen ja kaasun diffuusiopolton aikana ovat samojen lakien alaisia, koska molemmissa tapauksissa palamisprosessin määrää polttoaineen ja hapettimen keskinäinen diffuusio. Jos kaasujen diffuusiopolton aikana kaasuvirran nopeus ei kuitenkaan riipu liekissä tapahtuvista prosesseista, niin nesteen palamisen aikana muodostuu tietty palamisnopeus, joka riippuu sekä nesteen termodynaamisista parametreista että ilman hapen ja nestehöyryn diffuusioolosuhteista.
Palamisvyöhykkeen ja nesteen pinnan välille muodostuu tietty lämmön ja massan siirto (kuva 2.6). Osa lämpövirrasta, joka saavuttaa nesteen pinnan q 0v kuluu sen lämmittämiseen kiehumispisteeseen q ucn. Lisäksi se on lämmin qCT Neste syötetään lämmittämään liekistä säiliön seinien läpi lämmönjohtavuuden vuoksi. Riittävän suurella halkaisijalla qCT voidaan sitten jättää huomiotta q() = K „n +
Se on selvää
missä c on nesteen lämpökapasiteetti, kJDkg-K); p - nesteen tiheys, kg/m3; Wnc- lämmitetyn kerroksen kasvunopeus, m/s; W Jl - lineaarinen palamisnopeus, m/s; 0 ja SP - höyrystymislämpö, kJ/kg; G kip on nesteen kiehumispiste K.

Riisi. 2.6.
Г () - alkulämpötila; G kiehua - kiehumispiste;
T g- palamislämpötila; q KUW q Jl - konvektiiviset ja säteilylämpövirrat, vastaavasti; q 0 - nesteen pinnalle saapuva lämpövirta
Kaavasta (2.45) seuraa, että liekkivyöhykkeeltä tulevan lämpövirran intensiteetti määrää tietyn polttoaineen syöttönopeuden tälle vyöhykkeelle, jonka kemiallinen vuorovaikutus hapettimen kanssa puolestaan vaikuttaa arvoon #0. Tämä on mitä massa- Ja lämmönvaihto liekkivyöhykkeen ja kondensoituneen faasin välillä nesteiden ja kiinteiden aineiden palamisen aikana.
Arvio lämmön osuudesta nesteen palamisen aikana vapautuvasta kokonaislämmöstä, joka kuluu sen valmistukseen palamista varten q 0 voidaan tehdä seuraavassa järjestyksessä.
Yksinkertaisuuden vuoksi W rjl= W nx , saamme
Lämmön vapautumisnopeus nestepinnan pinta-alayksikköä kohti (palon ominaislämpö qll7K) voidaan määrittää kaavalla
missä Q H on aineen alempi palamislämpö, kJ/kg; R p - palamistehokerroin.
Sitten, kun otetaan huomioon tila (2.44) ja jaetaan lauseke (2.45) kaavalla (2.46), saadaan
Laskelmat osoittavat, että noin 2 % kokonaislämmöstä nesteen palamisen aikana kuluu nestehöyryn muodostukseen ja toimittamiseen palamisalueelle. Kun palamisprosessi saadaan aikaan, nesteen pintalämpötila nousee kiehumispisteeseen, joka pysyy sen jälkeen ennallaan. Tämä lausunto koskee yksittäistä nestettä. Jos tarkastellaan eri kiehumispisteiden nesteiden seoksia, niin alhaalla kiehuvat jakeet tulevat ulos ensin, sitten yhä korkeammalla kiehuvat.
Palamisen nopeuteen vaikuttaa merkittävästi nesteen lämpeneminen syvyydessä lämmönsiirron seurauksena säteilyvirran lämmittämästä nesteestä q 0 nesteen pintaa sen syvyyteen. Tämä lämmönsiirto tapahtuu johtuen lämmönjohtokyky Ja yleissopimus.
Lämmönjohtavuudesta johtuva nesteen kuumeneminen voidaan esittää muodon eksponentiaalisella riippuvuudella
Missä T x - nestekerroksen lämpötila syvyydessä X, TO; G kip - pintalämpötila (kiehumispiste), K; k- suhteellisuuskerroin, m -1.
Tämän tyyppistä lämpötilakenttää kutsutaan ensimmäisen tyyppinen lämpötilajakauma(Kuva 2.7).
Laminaarikonventio syntyy nesteen erilaisista lämpötiloista säiliön seinillä ja sen keskellä sekä ylemmässä kerroksessa tapahtuvasta jakotislauksesta seoksen palamisen aikana.
Lisälämmönsiirto säiliön lämmitetyistä seinistä nesteeseen johtaa sen seinien lähellä olevien kerrosten kuumenemiseen korkeampaan lämpötilaan kuin keskellä. Seinien lähellä kuumennettu neste (tai jopa höyrykuplat, jos se kuumennetaan seinillä kiehumispisteen yläpuolelle) nousee, mikä edistää intensiivistä sekoittumista ja nesteen nopeaa kuumenemista suurissa syvyyksissä. Niin kutsuttu homoterminen kerros, nuo. lähes vakiolämpötilainen kerros, jonka paksuus kasvaa palamisen aikana. Tätä lämpötilakenttää kutsutaan toisen tyyppinen lämpötilajakauma.

Riisi. 2.7.
1 - ensimmäisen tyyppinen lämpötilajakauma; 2 - toisen tyyppinen lämpötilajakauma
Homotermisen kerroksen muodostuminen on mahdollista myös eri kiehumispisteiden omaavien nesteiden seoksen pintaa lähellä olevien kerrosten jakotislauksen tuloksena. Kun tällaiset nesteet palavat, pintakerros rikastuu tiheämmillä, korkealla kiehuvilla fraktioilla, jotka uppoavat, mikä helpottaa nesteen konvektiivista kuumenemista.
On todettu, että mitä alhaisempi nesteen (dieselpolttoaine, muuntajaöljy) kiehumispiste on, sitä vaikeampaa on homotermisen kerroksen muodostuminen. Kun ne palavat, säiliön seinämien lämpötila ylittää harvoin kiehumispisteen. Kuitenkin, kun poltetaan märkiä korkealla kiehuvia öljytuotteita, homotermisen kerroksen muodostumisen todennäköisyys on melko suuri. Kun säiliön seinämät kuumennetaan 100°C:een tai korkeampaan lämpötilaan, muodostuu vesihöyrykuplia, jotka ryntäessään ylöspäin aiheuttavat kaiken nesteen voimakasta liikettä ja nopeaa lämpenemistä syvyydessä. Homotermisen kerroksen paksuuden riippuvuutta palamisajasta kuvaa suhde
Missä X - homotermisen kerroksen paksuus jossain vaiheessa palamisaikaa, m; x pr - homotermisen kerroksen maksimipaksuus, m; t on aika, joka lasketaan siitä hetkestä, kun kerros alkaa muodostua, s; p - kerroin, s -1.
Mahdollisuus riittävän paksun homotermisen kerroksen muodostumiseen märkien öljytuotteiden palamisen aikana on täynnä kiehumista ja nesteen purkamista.
Palamisnopeus riippuu merkittävästi nestetyypistä, alkulämpötilasta, kosteudesta ja ilmakehän happipitoisuudesta.
Yhtälöstä (2.45) ottaen huomioon lausekkeen (2.44) voidaan määrittää massapalamisnopeus:

Kaavasta (2.50) käy ilmi, että palamisnopeuteen vaikuttavat liekistä nestepinnalle tulevan lämpövirran intensiteetti ja polttoaineen termofysikaaliset parametrit: kiehumispiste, lämpökapasiteetti ja haihtumislämpö.
Pöydältä 2.5 on ilmeistä, että palamisnopeuden ja nesteen lämmittämiseen ja haihduttamiseen tarvittavan lämmönkulutuksen välillä on tietty vastaavuus. Siten bentseeneksyleeniglyserolien sarjassa, kun lämmönkulutus kasvaa lämmitykseen ja haihdutukseen, palamisnopeus laskee. Kuitenkin siirryttäessä bentseenistä dietyylieetteriin lämpökustannukset pienenevät. Tämä ilmeinen ero johtuu polttimesta nesteen pintaan tulevien lämpövirtojen intensiteetin eroista. Säteilyvirta on riittävän suuri bentseenin savuiselle liekille ja pieni dietyylieetterin suhteellisen läpinäkyvälle liekille. Pääsääntöisesti nopeimmin palavien nesteiden ja hitaimmin palavien nesteiden palamisasteiden suhde on melko pieni ja on 3,0-4,5.
Taulukko 25
Palamisnopeuden riippuvuus lämmönkulutuksesta lämmitykseen ja haihdutukseen
Lausekkeesta (2.50) seuraa, että G 0:n kasvaessa palamisnopeus kasvaa, koska lämmönkulutus nesteen lämmittämiseksi kiehumispisteeseen pienenee.
Seoksen kosteuspitoisuus vähentää nesteen palamisen nopeutta ensinnäkin sen haihtumisen lisälämmönkulutuksen vuoksi ja toiseksi vesihöyryn flegmatisoivan vaikutuksen seurauksena kaasuvyöhykkeessä. Jälkimmäinen johtaa liekin lämpötilan laskuun, ja siksi kaavan (2.43) mukaan myös sen emissiokyky pienenee. Tarkkaan ottaen märän nesteen (vettä sisältävän nesteen) palamisnopeus ei ole vakio, se kasvaa tai laskee palamisprosessin aikana riippuen nesteen kiehumispisteestä.
Märkä polttoaine voidaan esittää kahden nesteen seoksena: polttoaine + vesi, jonka palamisprosessissa niiden jakotislaus. Jos syttyvän nesteen kiehumispiste on alhaisempi kuin veden kiehumispiste (100°C), tapahtuu polttoaineen ensisijainen palaminen, seos rikastuu vedellä, palamisnopeus laskee ja lopuksi palaminen pysähtyy. Jos nesteen kiehumispiste on yli 100 °C, kosteus päinvastoin ensin haihtuu ja sen pitoisuus pienenee. Tämän seurauksena nesteen palamisnopeus kasvaa puhtaan tuotteen palamisnopeuteen asti.
Yleensä tuulen nopeuden kasvaessa nesteen palamisen nopeus kasvaa. Tuuli tehostaa polttoaineen sekoittumisprosessia hapettimeen, mikä nostaa liekin lämpötilaa (taulukko 2.6) ja tuo liekin lähemmäs palamispintaa.
Taulukko 2.6
Tuulen nopeuden vaikutus liekin lämpötilaan
Kaikki tämä lisää nesteen lämmittämiseen ja haihduttamiseen syötettävän lämpövirran intensiteettiä, mikä lisää palamisnopeutta. Suuremmilla tuulennopeuksilla liekki voi murtua, mikä johtaa palamisen lakkaamiseen. Esimerkiksi traktorin kerosiinin palaessa halkaisijaltaan 3 m:n säiliössä liekki sammui tuulen nopeudella 22 m/s.
Useimmat nesteet eivät voi palaa ilmakehässä, jossa on alle 15 % happea. Kun happipitoisuus nousee tämän rajan yläpuolelle, palamisnopeus kasvaa. Ilmakehässä, joka on merkittävästi rikastettu hapella, nesteen palaminen etenee, jolloin liekkiin vapautuu suuri määrä nokea ja nestefaasin kiehumista havaitaan. Monikomponenttisten nesteiden (bensiini, kerosiini jne.) pintalämpötila nousee ympäristön happipitoisuuden kasvaessa.
Palamisnopeuden ja nesteen pintalämpötilan nousu ilmakehän happipitoisuuden kasvaessa johtuu liekin emissiokyvyn kasvusta palamislämpötilan nousun ja sen korkean nokipitoisuuden seurauksena.
Palamisnopeus muuttuu myös merkittävästi, kun palavan nesteen taso säiliössä laskee: palamisnopeus laskee, kunnes palaminen lakkaa. Koska ilman hapen syöttö ympäristöstä säiliöön on vaikeaa, nesteen tason laskeessa etäisyys kasvaa h np liekkivyöhykkeen ja palamispinnan väliin (kuva 2.8). Säteilyvirtaus nestepeiliin pienenee ja sen seurauksena palamisnopeus pienenee, jopa vaimennuspisteeseen asti. Poltettaessa nesteitä halkaisijaltaan suurissa säiliöissä maksimi syvyys/g, jossa palamisen vaimennus tapahtuu, on erittäin suuri. Joten säiliölle, jonka halkaisija on 5 m, se on 11 m ja halkaisijaltaan Im noin 35 m.

Adiabaattisessa, ts. palamiseen ei liity lämpöhäviöitä, palavan järjestelmän koko kemiallisen energian tarjonta muunnetaan reaktiotuotteiden lämpöenergiaksi. Adiabaattisen palamistuotteiden lämpötila ei riipu liekissä tapahtuvien reaktioiden nopeudesta, vaan ainoastaan niiden kokonaislämpövaikutuksesta ja lopputuotteiden lämpökapasiteeteista. Tätä arvoa kutsutaan adiabaattiseksi palamislämpötilaksi T d. Se on palavan ympäristön tärkeä ominaisuus. Useimmille palaville seoksille arvo T g on alueella 1500 ÷ 3000°K. Se on selvää T d – reaktiotuotteiden maksimilämpötila ilman ulkoista kuumennusta. Palamistuotteiden todellinen lämpötila voi olla vain pienempi T d lämpöhäviön sattuessa.
Neuvostoliiton tutkijoiden Ya B. Zeldovichin ja D. A. Frank-Kamenetskyn kehittämän palamisen lämpöteorian mukaan liekki etenee siirtämällä lämpöä palamistuotteista palamattomaan (tuoreeseen) seokseen. Kaasuseoksen lämpötilajakauma, ottaen huomioon kemiallisesta reaktiosta vapautuva lämmön ja lämmönjohtavuus, on esitetty kuvassa. 6.1:
Riisi. 6.1. Lämpötilan jakautuminen kaasuseoksessa
Liekin etuosa, ts. vyöhyke, jossa palamisreaktio ja palamiskaasun voimakas itsekuumeneminen tapahtuu, alkaa itsesyttymislämpötilasta T St ja päättyy lämpötilaan T G.
Oikealle etenevän liekkirintaman edessä on tuore seos ja takana palamistuotteet. Uskotaan, että kuumennusvyöhykkeellä reaktio etenee niin hitaasti, että lämmön vapautuminen unohtuu.
Lämmönsiirtoprosessi paikallaan olevan liekin leviämisen aikana ei johda lämpöhäviöön ja lämpötilan laskuun verrattuna T d suoraan liekin etuosan takana. Lämmönpoisto kustakin palavasta kaasukerroksesta, kun viereinen, vielä lämmittämätön sytytetään, kompensoidaan vastaavalla määrällä lämpöä, joka on tullut aikaisemmin sytytyskerrokseen oman syttymisensä aikana. Alkusytytyspulssin lisälämpö ei merkittävästi vääristä vakaan tilan palamisjärjestelmää, koska sen rooli pienenee yhä enemmän poltetun kaasun määrän kasvaessa.
Palamistuotteet menettävät lämpöä vain säteilyn seurauksena ja joutuessaan kosketuksiin kiinteän pinnan kanssa. Jos säteily on merkityksetöntä, tällainen palaminen osoittautuu käytännössä adiabaattiseksi. Huomattavat lämpöhäviöt ovat mahdollisia vain tietyllä etäisyydellä liekkirintaman takana.
Siten kaasuseoksen palamisen käynnistyminen yhdessä kohdassa johtaa läheisen kerroksen kuumenemiseen, jota kuumennetaan reaktiotuotteista peräisin olevan lämmön johdosta itsesyttymiseen asti. Tämän kerroksen palaminen edellyttää seuraavan kerroksen syttymistä jne. kunnes palava seos palaa kokonaan. Reaktiovyöhykkeestä tuoreeseen seokseen poistunut lämpö kompensoituu täydellisesti reaktiolämmön vapautumisella ja syntyy vakaa liekkirintama. Kerros kerrokselta palamisen seurauksena liekin etuosa liikkuu seoksen läpi, jolloin liekki pääsee leviämään.
Jos tuore seos liikkuu kohti liekin rintamaa nopeudella, joka on yhtä suuri kuin liekin etenemisnopeus, niin liekki on liikkumaton (pysähdyksissä).
Tuoreeseen seokseen syötetään määrä lämpöä liekin pintayksiköstä aikayksikköä kohden lämmönjohtavuudella:
![]() (6.7)
(6.7)
missä on lämmönjohtavuuskerroin; – liekin etuosan leveys.
Tämä lämpö kuluu tuoreen seoksen lämmittämiseen alkulämpötilasta palamislämpötilaan:
Missä Kanssa- ominaislämpökapasiteetti; – seoksen tiheys.
Ottaen huomioon yhtälöt (6.7) ja (6.8) kohdassa U pl =υ g liekin etenemisnopeus määräytyy suhteella:
 , (6.9)
, (6.9)
missä on lämpödiffuusiokerroin.
Koska palamisnopeus riippuu suuresti lämpötilasta, kaasun suurin osa palaa vyöhykkeellä, jonka lämpötila on lähellä
Kemiallisen reaktion nopeus määräytyy yhtälöllä:
(6.10)
Silloin liekin etenemisnopeus on:
 (6.11)
(6.11)
Missä b– indikaattori, joka riippuu seoksen ominaisuuksista.
Näin ollen liekki ei pääse leviämään palavan seoksen läpi, jos sen lämpötila on jonkin verran alle teoreettisen palamislämpötilan.
Suurin liekin etenemisnopeus Ei havaita polttoaineen ja hapettimen stoikiometrisellä suhteella seoksessa, vaan polttoaineen ylimäärällä. Seosta esilämmitettäessä liekin etenemisnopeus todellisissa olosuhteissa kasvaa merkittävästi, koska se on verrannollinen seoksen alkulämpötilan neliöön.
Normaali liekin etenemisnopeus (un) riippuu kaasu-ilma-seoksen lämpöfysikaalisista ominaisuuksista. Mutta vielä suuremmassa määrin riippuu leviämisnopeus sen fysikaalis-kemiallisista ominaisuuksista? palamisnopeus V ja lämpötila palamisreaktioalueella, TG:
nuo. un on verrannollinen hapetusreaktion nopeuteen (V) ja on eksponentiaalisesti riippuvainen palamisvyöhykkeen käänteislämpötilasta (Tg). Ratkaiseva parametri on tietysti reaktionopeus. Kirjoita kemiallisen palamisreaktion nopeuden yhtälö:

jossa k0 on Arrhenius-yhtälön esieksponentiaalinen tekijä,
Cg, mehu - polttoaineen ja hapettimen pitoisuudet,
m, n - polttoaineen ja hapettimen reaktiomääräykset, vastaavasti,
Ea on kemiallisen reaktion aktivointienergia.
Tarkastellaan kuinka hapetusreaktioiden nopeus muuttuu seoksissa, joissa on eri polttoaineen ja hapettimen suhde (kuva 2).
Kaavio osoittaa, että stoikiometrisen koostumuksen seoksella (ilman ylimääräkerroin? = 1) hapetusreaktion nopeus on suurin.
Milloin polttoaineen pitoisuus seoksessa nousee stoikiometrisen määrän yläpuolelle? tulee< 1 (кислород находится в недостатке), горючее сгорает не полностью. В этом случае меньше выделится теплоты реакции горения Qгор и произойдёт снижение Tг.
Hapetusreaktion nopeus laskee verrattuna seoksen stoikiometriseen koostumukseen, johtuen sekä hapettimen 02 pitoisuuden laskusta että palamisvyöhykkeen lämpötilasta. Eli jatkuvalla laskulla? (joka vastaa SG:n pitoisuuden lisäämistä seoksessa) hapetusreaktion nopeus? ja paloalueen lämpötilat Tg laskevat jatkuvasti. Kuvaajalla SG > SGstech käyrä tulee jyrkästi alaspäin. Hapettumisreaktion nopeuden lasku? > 1 selittyy lämmön vapautumisen vähenemisellä palamisvyöhykkeellä, koska siinä on pienempi polttoainepitoisuus.

Kuva 2. Palamisnopeuden riippuvuus polttoaineen pitoisuudesta seoksessa
Se on täsmälleen sama kuin kuvassa 2, palamisreaktion nopeuden riippuvuus palavan komponentin pitoisuudesta alkuperäisessä seoksessa, joka määrää ennalta sen muiden palamisprosessin parametrien riippuvuuden parabolisen muodon palamisprosessin koostumuksesta. seos: itsesyttymislämpötila ja minimisytytysenergia, liekin etenemisen pitoisuusrajat. Normaalin liekin etenemisnopeuden un riippuvuus polttoaineen pitoisuudesta SG-seoksessa on myös paraabelin muotoinen. Kuvassa Kuvassa 3 on esitetty tällaiset riippuvuudet ilma-propaaniseoksen palaessa alkulämpötilan eri arvoilla.

Kuva 3. Liekin etenemisnopeuden riippuvuus propaanipitoisuudesta ilmassa alkulämpötilassa 311 K (1); 644 K (2); 811 K (3)
Yllä kuvattujen käsitteiden mukaan liekin enimmäisetenemisnopeuden (unmax) tulee vastata polttoaineen stoikiometristä pitoisuutta. Sen kokeellisesti löydetyt arvot ovat kuitenkin hieman siirtyneet kohti runsaasti palavia seoksia. Seoksen alkulämpötilan noustessa liekin etenemisnopeuden tulisi kasvaa, mitä käytännössä havaitaan. Esimerkiksi bensiinin ja kerosiinihöyryjen ilmaseokselle sen muoto on kuvan 1 mukainen. 4.

Kuva 4. Liekin etenemisnopeuden riippuvuus bensiinin ja kerosiinihöyryjen ilmaseoksen alkulämpötilasta
Eri aineiden kohdalla u riippuu niiden kemiallisesta luonteesta ja vaihtelee melko laajoissa rajoissa (taulukko 1). Useimmille hiilivetypolttoaineiden ja ilman seoksille< 1 м/с. При введении в горючую смесь избыточного воздуха или азота температура горения заметно снижается.
Pöytä 1.
Normaali liekin etenemisnopeus joillekin syttyville seoksille
Inerttien ja neutraalien kaasujen syöttäminen palavaan seokseen: typpi N2, argon Ar, hiilidioksidi CO2 laimentaa sitä ja vähentää siten sekä hapetusreaktion nopeutta että liekin etenemisnopeutta. Tämä näkyy selvästi kuvassa esitetyistä riippuvuuksista. 5.
Lisäksi tietyllä (flegmatisoivalla) laimennusainepitoisuudella palaminen lakkaa kokonaan. Freonien käyttöönotolla on voimakkain vaikutus, koska niillä on myös estävä vaikutus palamisreaktioon.
Kuten kuvasta voidaan nähdä. 5, freonin (114B2) lisääminen palavaan seokseen on 4 - 10 kertaa tehokkaampi kuin neutraalit kaasut - laimentimet.

Kuva 5. Laimennusaineiden ja kylmäaineen 114B2 pitoisuuden vaikutus liekin etenemisnopeuteen propaani-ilmaseoksessa (? = 1,15)
Laimennuskaasujen flegmatisointikyky riippuu niiden lämpöfysikaalisista ominaisuuksista ja erityisesti niiden lämmönjohtavuudesta ja lämpökapasiteetista.
1.3 Kaasujen diffuusiopoltto
Todellisissa olosuhteissa, kun kaasu tai höyry syttyy niiden hätäulosvirtauksen alkamisen jälkeen, havaitaan diffuusiopoltto. Tyypillinen ja melko yleinen esimerkki on kaasun diffuusiopoltto pääputkien tuhoutumisen yhteydessä, kaasun tai kaasun lauhdekentän merellä tai maissa hätäpursuavassa kaivossa kaasunkäsittelylaitoksissa.
Tarkastellaanpa tällaisen palamisen ominaisuuksia. Oletetaan, että palaa maakaasulähde, jonka pääkomponentti on metaani. Palaminen tapahtuu diffuusiotilassa ja on luonteeltaan laminaarista. Metaanin liekin leviämisen (CPLP) pitoisuusrajat ovat 5 - 15 tilavuusprosenttia. Kuvataan liekin rakenne ja rakennetaan graafiset riippuvuudet metaanipitoisuuden muutoksesta ja palamisreaktion nopeudesta etäisyydestä aksiaaliseen suihkulähteeseen (kuva 6).

Kuva 6. Kaavio kaasulähteen diffuusiolaminaariliekistä (a), polttoainepitoisuuden muutoksesta (b) ja palamisreaktionopeudesta (c) liekin rintamalla.
Kaasupitoisuus laskee 100 %:sta aksiaalisessa suihkulähteessä syttymisen ylärajan arvoon ja edelleen LFL:ään sen reunalla.
Kaasun palaminen tapahtuu vain pitoisuusalueella VKPR:stä LKPR:ään, eli. syttymisen pitoisuusalueella. Palamisreaktion nopeus (T) on nolla pitoisuuksilla, jotka ovat VKPR:n yläpuolella ja LKPR:n alapuolella, ja maksimi klo. Siten HNKPR:n ja HVKPR:n välinen etäisyys määrää diffuusioliekin eturintaman leveyden:
fp = HNKPR - HVKPR. (3)
Tällaisen liekin etuleveys on 0,1 - 10 mm. Palamisreaktion nopeus tässä tapauksessa määräytyy hapen diffuusionopeuden mukaan ja sen arvo on noin 5×104 kertaa pienempi kuin palamisnopeus kineettisessä tilassa. Lämpöintensiteetti on yhtä monta kertaa pienempi, ts. lämmön vapautumisnopeus diffuusiopolttopolttimessa.
1.4 Kaasusuihkujen palamisen ominaisuudet. Liekin stabilointiolosuhteet
Kaasusuihkulähteiden palamisolosuhteita on helpompi tarkastella kaasusuihkujen esimerkin avulla. Todellisissa olosuhteissa tällaiset suihkut ovat turbulentteja. Kun kaivosta virtaava kaasuvirta sytytetään, muodostuu ns. diffuusiopilvi, jolla on symmetrinen karan muotoinen muoto (kuva 6). Kemialliset palamisreaktiot tapahtuvat polttimen ohuessa pintakerroksessa, jota voidaan ensimmäisen likiarvon mukaan pitää pintana, jossa polttoaineen ja hapettimen pitoisuudet nousevat ja polttoaineen ja hapettimen diffuusiovirrat tälle pinnalle ovat stoikiometrisesti. suhde. Diffuusiopolttorintaman etenemisnopeus on nolla, joten se ei voi pysyä itsenäisesti ylöspäin virtaavan suihkun päällä.
Liekin stabiloituminen suihkussa tapahtuu polttimen alaosassa, jossa toteutetaan toinen palamismekanismi. Kun kaasua virtaa ulos reiästä, muodostuu pyörteinen kerros sekoittuvaa kaasua ja ympäröivää ilmaa suihkupinnan alkuperäiselle palamattomalle alueelle. Tässä kerroksessa kaasupitoisuus säteen suunnassa vähitellen laskee ja hapettimen pitoisuus kasvaa. Sekoituskerroksen keskiosaan ilmestyy homogeeninen polttoaineen ja hapettimen seos, jonka koostumus on lähellä stoikiometristä. Kun tällainen palamiseen valmisteltu seos sytytetään, liekinrintama voi edetä sekoituskerroksessa rajallisella nopeudella, jopa virtausta kohti, jos palamisnopeus ylittää paikallisen virtausnopeuden. Mutta koska suihkun nopeus kasvaa lähestyttäessä poistoaukkoa, tietyllä korkeudella suihkun nopeus (uf) tulee yhtä suureksi kuin palamisnopeus (at), ja liekki stabiloituu suihkun pinnalle tällä korkeudella. Turbulenttisen palamisen nopeutta (?t) ei ole mahdollista laskea tarkasti. Arviot kuitenkin osoittavat, että arvo (At) on suunnilleen yhtä suuri kuin suihkun sykkimisnopeudet, joiden suuruus on verrannollinen aksiaaliseen nopeuteen (um). Kokeellisista tiedoista seuraa, että pituussuuntaisen nopeuskomponentin neliökeskiarvopulsaatioiden maksimiarvot ovat 0,2 um. Kun tämä arvo otetaan pyörteisen palamisen nopeudeksi, voidaan olettaa, että liekin suurin etenemisnopeus kohti nopeudella 300-450 m/s pursuttavaa kaasusuihkua on noin 50 m/s.
1.5 Palavien kaasusuihkulähteiden virtausnopeuden arviointi
Sammutettaessa tulipaloja voimakkaista kaasusuihkulähteistä on tarpeen arvioida palavan suihkulähteen virtausnopeus (D), koska kaasun kulutus on yksi tärkeimmistä parametreista, jotka määräävät työmäärän sekä onnettomuuden poistamiseen tarvittavat materiaali- ja tekniset keinot. . Palavan suihkulähteen virtausnopeuden suora mittaus osoittautuu kuitenkin useimmissa tapauksissa mahdottomaksi, eikä ole olemassa tehokkaita etämenetelmiä suihkun virtausnopeuden määrittämiseen. Voimakkaiden kaasusuihkulähteiden kulutus voidaan määrittää melko tarkasti taskulampun korkeudella (H).
Tiedetään, että normaalisti paisuneiden kaasusuihkujen palaessa aliääninopeudella muodostuvan turbulentin pölyn korkeus ei riipu suihkun nopeudesta tai virtausnopeudesta, vaan sen määrää vain reiän halkaisija (d). josta suihku virtaa, kaasun lämpöfysikaaliset ominaisuudet ja sen lämpötila (T) reiän ulostulossa.
On olemassa hyvin tunnettu empiirinen kaava suihkulähteen virtausnopeuden laskemiseksi polttimen korkeuden perusteella maakaasua poltettaessa:
D = 0,0025Hf 2 milj. m3/vrk. (4)
Todellisissa tulipaloissa laminaarista palamista ei käytännössä tapahdu. Kaasu sekä kaasukentän säiliössä että kuljetusputkissa ja teknologisissa laitteistoissa on paineen alaisena. Siksi kaasunkulutus hätävuodon aikana on erittäin korkea? 100 m3/s asti vuotavien kaasukaivojen tulipaloissa (jopa 10 milj. m3/vrk). Luonnollisesti näissä olosuhteissa ulosvirtaustilat ja siten myös palamistilat ovat turbulentteja.
Voimien ja keinojen laskemiseksi palavien kaasusoihduksien sammuttamiseksi on tiedettävä kaasun kulutus. Alkutiedot sen laskemista varten puuttuvat lähes aina, koska joko kaasun painetta prosessilaitteistossa tai kentän säiliössä ei tunneta. Siksi käytännössä he käyttävät polttimen liekin korkeuden kokeellisesti määritettyä riippuvuutta (4) kaasun virtausnopeudesta, jonka laskennalliset tiedot on annettu taulukossa. 2.
Taulukko 2.
Liekin korkeuden riippuvuus kaasulähteen kaasuvirtauksesta eri palamismuodoissa
